Orbital nguyên tử (tiếng Anh: atomic orbital, viết tắt AO) hay obitan nguyên tử, quỹ đạo nguyên tử là một hàm toán học mô tả lại trạng thái như sóng điện từ của một electron.[1] Hàm này được dùng để tính toán xác suất tìm thấy electron của một nguyên tử ở bất kì chỗ nào bao quanh không gian hạt nhân của nguyên tử. Những hàm này có thể cung cấp một biểu đồ (đồ thị) ba chiều của các vị trí có khả năng có một electron. Giới hạn có thể xác định được theo vùng của vật chất từ hàm mà có khả năng tìm được electron.[2] Một cách cụ thể hơn, những orbital nguyên tử có những trạng thái lượng tử của một cá nhân electron trong một tập hợp electron bao quanh một đơn nguyên tử, như được mô tả từ hàm quỹ đạo (orbital function).
Mặc dù điều này giống với các hành tinh quay xung quanh Mặt trời, các electron không thể mô tả như những hạt rắn và vì thế mới có tên gọi là orbital nguyên tử. Từ trước, con người nghĩ quỹ đạo nguyên tử tương tự như quỹ đạo hình elip của các hành tinh. Một cách nói chính xác hơn là một đám bụi lớn và thường có khí quyển với hình thù kì quặc (là tập hợp các hạt electron), phân bố xung quanh một hành tinh tương đối nhỏ (là hạt nhân nguyên tử). Nếu chính xác thì các orbital nguyên tử được mô tả như hình dạng của bầu khí quyển chỉ khi một electron độc thân (single ectron) có mặt trong một nguyên tử. Khi có nhiều electron được thêm vào một nguyên tử độc thân, sự bổ sung thêm các electron đó tạo nên sự đồng đều để lấp đầy vùng không gian xung quanh hạt nhân (đôi khi còn gọi là "đám mây electron" của nguyên tử[3]) dẫn đến một khối hình cầu trong đó xác suất tìm thấy electron càng ngày càng lớn.

Ý tưởng đưa ra điều các electron có thể quay xung quanh hạt nhân được xác định với thuyết mô men động lượng của Niels Bohr vào năm 1913,[4] và một nhà vật lý người Nhật Bản Hantaro Nagaoka đưa ra giả thuyết sự chuyển động của electron từ khá sớm vào năm 1904.[5] Tuy nhiên, giả thuyêt này không được chấp nhận cho đến năm 1926 mới có một giả thuyết mới từ phương trình Schrödinger về các sóng trạng thái electron trong nguyên tử cung cấp một số hàm cho những orbital hiện đại (modern orbitals).[6]
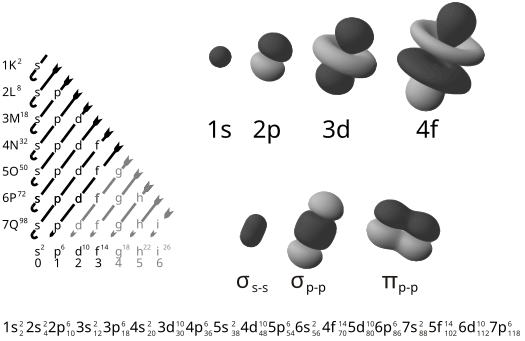
Do sự khác biệt với loại quỹ đạo cổ điển, thuật ngữ "quỹ đạo" (orbit) của các electron trong nguyên tử đã được thay bằng thuật ngữ "orbital" (orbital, loại tính từ), từ này được đặt ra đầu tiên bởi nhà hoá học Robert Mulliken vào năm 1932.[7] Orbital nguyên tử thường được mô tả giống như các hàm sóng (wave functions) kiểu hydro (nghĩa là một electron) qua không gian, phân loại theo n, l, và m số lượng tử, tương ứng với các năng lượng của electron, mô men động lượng và phương của mô men động lượng, tuỳ theo. Mỗi orbital được xác định theo số lượng tử khác nhau và có tối đa là hai electron. Có tên gọi đơn giản là orbital s, orbital p, orbital d, và orbital f tham gia vào các loại orbital (orbitals) của số lượng tử mô men động lượng l = 0, 1, 2 và 3 theo tương ứng. Những loại tên này chỉ ra hình dạng của orbital và được sử dụng để diễn tả cấu hình nguyên tử như ở hình bên phải. Các ký tự s, p, d, f đều được bắt nguồn từ các đặc tính của các dòng quang phổ của chúng: sharp (sắc nét), principal (chính, chủ yếu), diffuse (tán xạ), và fundamental (cơ bản, cơ sở), phần còn lại được đặt theo bảng chữ cái alphabe (ngoại từ ký tự j).[8][9]
Từ khoảng năm 1920, ngay trước khi nền cơ học lượng tử hiện đại và quy tắc aufbau ra đời thì nguyên tử được tạo dựng nên từ các cặp electron, được sắp xếp đơn giản lặp đi lặp lại theo mô hình số lẻ (1, 3, 5, 7...), đã được gợi lên bởi Niels Bohr và một số người tham gia khác có chút giống với orbital nguyên tử trong cấu hình electron của các nguyên tử phúc tạp. Trong toán học của vật lý nguyên tử, nó được dùng để giới thiệu về các hàm điện tử của các hệ thống phức tạp vào trong sự kết hợp với sự đơn giản của orbital nguyên tử. Mặc dù mỗi electron trong một đa electron nguyên tử không giới hạn trong một hoặc hai electron nguyên tử, vẫn còn hàm sóng lượng tử có thể bị phá vỡ khi vẫn còn trong orbital nguyên tử.
Mây electron của nguyên tử hydro ở trạng thái cơ bản hầu như tập trung trong vùng không gian có dạng hình cầu bán kính trung bình 0,053 nm.[10]
Những loại orbital được ký hiệu tên như sau:
trong đó X là mức năng lượng tương ứng với lượng tử số chính n (principal quantum number), type là một ký tự không viết hoa để chỉ hình dạng hoặc lớp phân vỏ của orbital và nó tương ứng với số lượng tử góc, l, và y là số electron trong orbital.
Ví dụ, orbital 1s2 có hai electron và mức năng lượng thấp nhất (n = 1). Trong phần ký hiệu X, lượng tử số chính chỉ thị một ký tự liên kế với nó. Đối với n = 1, 2, 3, 4, 5,..., thì các ký tự liên kết với những số đó là K, L, M, N, O,... theo tương ứng. orbital 1s2 có nghĩa là lớp 1, phân lớp s và có 2 electron.
Định nghĩa chính của cơ học lượng tử[sửa | sửa mã nguồn]
Trong cơ học lượng tử, trạng thái của một nguyên tử, tức là những trạng thái riêng của nguyên tử Hamilton, được mở rộng vào trong tổ hợp tuyến tinh của các sản phẩm theo nguyên tắc phản đối xứng của những hàm electron riêng biệt. Các thành phần có trong không gian của những hàm electron riêng biệt được gọi là orbital nguyên tử. (Khi xét qua thành phần spin (quay), một cách nói khác của orbital nguyên tử spin).
Trong vật lý nguyên tử, các vòng quang phổ nguyên tử tương ứng với trình chuyển đổi (bước nhảy lượng tử) giữa các trạng thái lượng tử của một nguyên tử. Các trạng thái này được ký hiệu bởi tập hợp số lượng tử được tóm tắt trong biểu tượng thuật ngữ và thường liên quan đến cấu hình đặc biệt của electron.
Không thể sử dụng vị trí và động năng để mô tả chuyển động của các electron xung quanh hạt nhân bởi chúng mang bản chất cơ học lượng tử. Thay vào đó chúng được mô tả bằng một nhóm các số lượng tử trong đó bảo gồm cả tính chất sóng và tính chất hạt của electron.
Mỗi orbital nguyên tử được xác định bởi một và chỉ một bộ ba giá trị của ba số lượng tử. Mỗi bộ ba giá trị này xác định một và chỉ một orbital, nhưng các số lượng tử chỉ xuất hiện theo các bộ giá trị nhất định. Các số lượng tử tuân theo các quy luật sau đây:
Số lượng tử chính n xác định năng lượng của electron và luôn là một số nguyên dương. n có thể là bất cứ số nguyên dương nào, nhưng những số lớn rất hiếm bắt gặp vì những lý do được trình bày bên dưới. Nói chung trong một nguyên tử, mỗi giá trị của n ứng với nhiều orbital. Những orbital này được gọi chung là các lớp vỏ electron.
Số lượng tử xung lượng l xác định moment góc của mỗi electron trong một orbital và luôn là một số nguyên không âm. Trong một lớp vỏ electron nào đó (n = n0), l có thể lấy bất cứ giá trị nguyên nào thỏa mãn 0 <= l <= n0 - 1. Ví dụ, lớp vỏ n = 1 chỉ có duy nhất một orbital với l = 0. Lơp vỏ n = 2 chỉ có hai orbital với l = 0 và l = 1. Nhóm các orbital có cùng giá trị của l được gọi chung là các lớp vỏ electron thứ cấp.
Liên hệ đến hệ thức bất định[sửa | sửa mã nguồn]
- orbital s có dạng hình cầu, tâm là hạt nhân nguyên tử.
- orbital p gồm 3 orbital px, py và pz có dạng hình số 8 nổi. Mỗi orbital có sự định hướng khác nhau trong không gian, chẳng hạn như orbital px định hướng theo trục x, orbital py định hướng theo trục y,...
orbital d,f có hình dạng phức tạp hơn.
Mỗi orbital có một mức năng lượng riêng
Các e trên mỗi orbital có một mức năng lượng xác định gọi là mức năng lượng orbital nguyên tử (mức năng lượng AO)
Các e trên các orbital khác nhau của cùng một phân lớp có năng lượng như nhau.
| Wikimedia Commons có thư viện hình ảnh và phương tiện truyền tải về Orbital nguyên tử |
- ^ Milton Orchin,Roger S. Macomber, Allan Pinhas, và R. Marshall Wilson (2005)"Thuyết orbital Nguyên tử"
- ^ Daintith, J. (2004). Từ điển Hóa Học Oxford. New York: Nhà Xuất Bản Đại Học Oxford. ISBN 0-19-860918-3.
- ^ Những bài giảng vật lý của Feynman - Xuất Bản Lần Cuối, Tập 1 bài 6 trang 11. Feynman, Richard; Leighton; Sands. (2006) Addison Wesley ISBN 0-8053-9046-4
- ^ Bohr, Niels (1913). “Tìm hiểu Cấu tạo của Nguyên tử và Phân tử”. Tạp chí Triết Học 26 (1): 476.
- ^ Nagaoka, Hantaro (tháng 5 năm 1904). “Kinetics of a System of Particles illustrating the Line and the Band Spectrum and the Phenomena of Radioactivity”. Philosophical Magazine 7: 445–455.
- ^ Bryson, Bill (2003). A Short History of Nearly Everything. Broadway Books. tr. 141–143. ISBN 0-7679-0818-X.
- ^ Mulliken, Robert S. (tháng 7 năm 1932). “Cấu trúc điện tử của Phân tử đa Nguyên tử và Hoá trị. II. General Considerations”. Vật lý. Rev. 41 (1): 49–71. doi:10.1103/PhysRev.41.49.
- ^ Griffiths, David (1995). Lời Giới thiệu về Cơ học Lượng tử. Prentice Hall. tr. 190–191. ISBN 0-13-124405-1.
- ^ Levine, Ira (2000). Cơ học Lượng tử (ấn bản 5). Prentice Hall. tr. 144–145. ISBN 0-13-685512-1.
- ^ Dẫn theo Sách Giáo Khoa Hoá Học lớp 10 của Nhà xuất bản Giáo dục

Comments
Post a Comment